获得紧急使用授权(EUA) 的COVID-19康复期血浆(CCP) 工具包
更新时间:2020年8月28日下午3:15
该工具包将持续更新。
请参阅第3页的新信息- AABB增加了关于COVID-19康复期血浆(CCP) 的紧急使用授权(EUA) 概述:
• 旨在帮助AABB成员直到获得美国食品和药物管理局(FDA) 的紧急使用授权(EUA) 指南出现
• 包括以下两项内容:
o 来自授权书的 紧急使用授权(EUA) 要求 ,以及
o 美国食品和药物管理局(FDA) 于2020年8月26日发布的指导意见。
与COVID-19康复期血浆(CCP) 紧急使用授权相关的信息变化迅速,会使得本次建议持续更新:
• 2020年5月1日,美国食品和药物管理局(FDA) 关于COVID-19康复期血浆(CCP) 的行业调查性指导,以及
• 美国食品和药物管理局(FDA) 的网站, 关于COVID-19康复期血浆的研究建议 。
新信息:
COVID-19康复期血浆(CCP) 的紧急使用授权(EUA) 概述,2020年8月28日下午3:15
概述如下,此处为链接:
• 旨在帮助AABB成员直到获得美国食品和药物管理局(FDA) 的紧急使用授权(EUA) 指南出现
• 包括以下两项内容:
o 来自授权书的 紧急使用授权(EUA) 要求 ,以及
o 美国食品和药物管理局(FDA) 于2020年8月26日发布的指导意见。
2020年8月23日事件
1- 美国食品和药物管理局(FDA) 提供了以下声明:
“一种针对COVID-19的探索性治疗方法是使用从COVID-19患者身上收集的康复期血浆治疗COVID-19。2020年8月23日,美国食品和药物管理局(FDA) 发布了COVID-19康复期血浆紧急使用授权(EUA)。此外,关于COVID-19康复期血浆的研究性建议页面提供了关于在紧急使用授权(EUA) 之外使用或研究COVID-19康复期血浆的途径信息。重要的是,继续招募和完成随机临床试验,以充分回答关于康复期血浆有效性的问题。医疗卫生机构或急救机构应从美国食品和药物管理局(FDA) 注册的血液机构获取COVID-19康复期血浆。”
2-紧急使用授权(EUA) 的COVID-19康复期血浆(CCP) 由防范和应对助理秘书办公室提供。
3- 美国食品和药物管理局(FDA) 新闻发布:FDA发布紧急使用授权,声明:
“今天,美国食品和药物管理局发布了用于治疗COVID-19住院患者的研究性康复期血浆的紧急使用授权(EUA),作为该机构抗击COVID-19的不懈努力的一部分。根据现有的科学证据,美国食品和药物管理局(FDA) 得出结论,正如其决策备忘录中概述的那样,该产品可能对治疗COVID-19有效,其已知和潜在的益处超过了该产品已知和潜在的风险。”
"紧急使用授权(EUA) 持续有效,直至证明有必要紧急使用药物和生物制剂预防和治疗COVID-19的情况出现后终止。如果确定紧急使用授权(EUA) 不再符合颁布的法定标准,则可对紧急使用授权(EUA) 进行修订或撤销。”
更多信息见新闻稿。
4- FDA发布了临床/决策备忘录-请参阅备忘录以获得支持这些结论的详细信息:
• COVID-19康复期血浆符合紧急使用授权资格标准。
• 对于紧急使用授权(EUA) 产品,COVID-19康复期血浆治疗COVID-19可能有效,而且有理由相信COVID-19康复期血浆(CCP) 已知和潜在的益处大于其已知和潜在的风险。
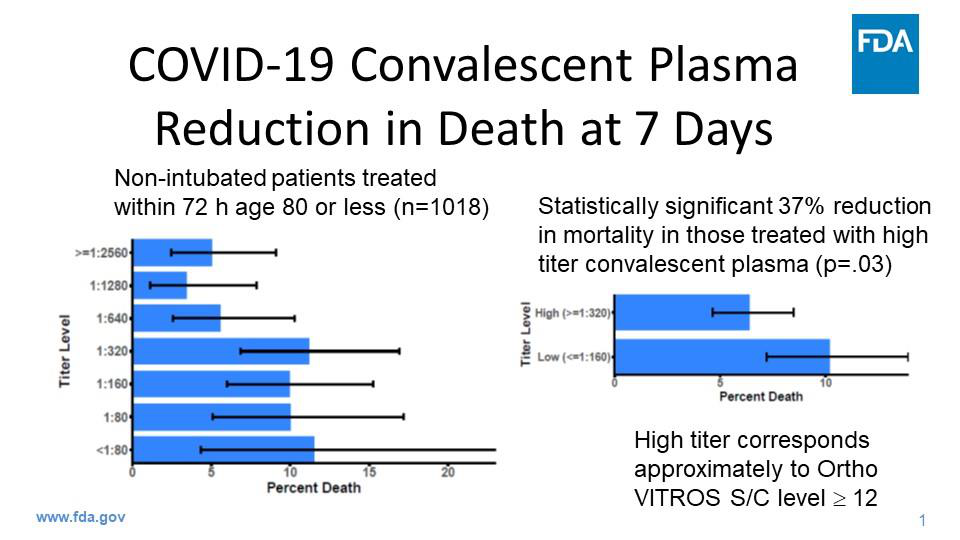
• 目前的证据表明,临床有效性最可能出现在早期治疗的患者 (例如,插管前)和使用具有较高抗体水平或中和作用的COVID-19康复期血浆(CCP) 。
• 目前的数据受到COVID-19康复期血浆(CCP) 的抗体水平或中和试验有效性的限制。根据现有数据,使用S/C临界值为12或更高的Ortho VITROS IgG测定法作为生成能力测试以鉴定CCP的高滴度单位是有依据的。
• 根据现有证据,在Ortho VITROS检测中,不超过12的CCP亦符合签发EUA的标准,因为有理由相信它可以有效的治疗COVID-19,且该产品已知和潜在的益处超过其已知和潜在的风险。这些单位血浆必须标记为“COVID-19低效价康复期血浆”。“医疗卫生机构可根据个人对潜在利益和风险的判断来决定是否使用这些血浆。
• 需要进行随机对照试验,以证明安全性和有效性,并确定使用COVID-19康复期血浆的最佳产品属性和适合的患者群体。
5-情况说明 — “紧急使用授权(EUA) 要求向医疗卫生机构和患者提供关于使用COVID-19康复期血浆治疗COVID-19重要信息的情况说明,包括剂量说明和潜在副作用。COVID-19康复期血浆可能产生的副作用包括过敏反应、输血相关的循环超负荷、输血相关的肺损伤、以及输血传播感染的可能性。”
• 为医疗卫生机构提供的情况介绍包括对产品的描述以及诸如药物相互作用、副作用、风险、效益和风险效益评估等信息。情况介绍还包括以下内容:
剂量
医疗卫生机构将根据标准的医院程序和机构医疗以及护理策略管理COVID-19康复期血浆。
临床剂量可首先考虑从一个康复期血浆单位(约200mL)开始输注,并根据处方医师的医学判断和患者的临床反应再给额外单位的康复期血浆。
心功能受损和心力衰竭患者可能需要更小的剂量或更长的输血时间。
管理
根据血浆管理的标准机构性医疗和护理策略,对通过外周静脉或中心静脉给予COVID-19康复期血浆的输注行为进行管理(http://www.aabb.org/tm/coi/Documents/coi1017.pdf)。
存储
COVID-19康复期血浆,可在-18℃或更低温度冷冻保存,有效期为收集之日起1年。一旦解冻,它可以在病人输血前复冷冻5天。
• 患者情况说明书为患者和患者父母/护理人员提供了基本信息。
6- EAP网站www.USCOVIDplasma.org发布了最新消息:
梅奥诊所主持的扩大准入项目将从当地时间2020年8月28日下午11:59分起停止新医生和新病人的登记。通过紧急使用授权,COVID-19康复期血浆仍可使用。
上海市血液中心 翻译:孙娟 审校:杨洁
附件:英文原版PDF 点击文件中的蓝字部分可以跳转阅读